PART 01
论文要点与研究主线
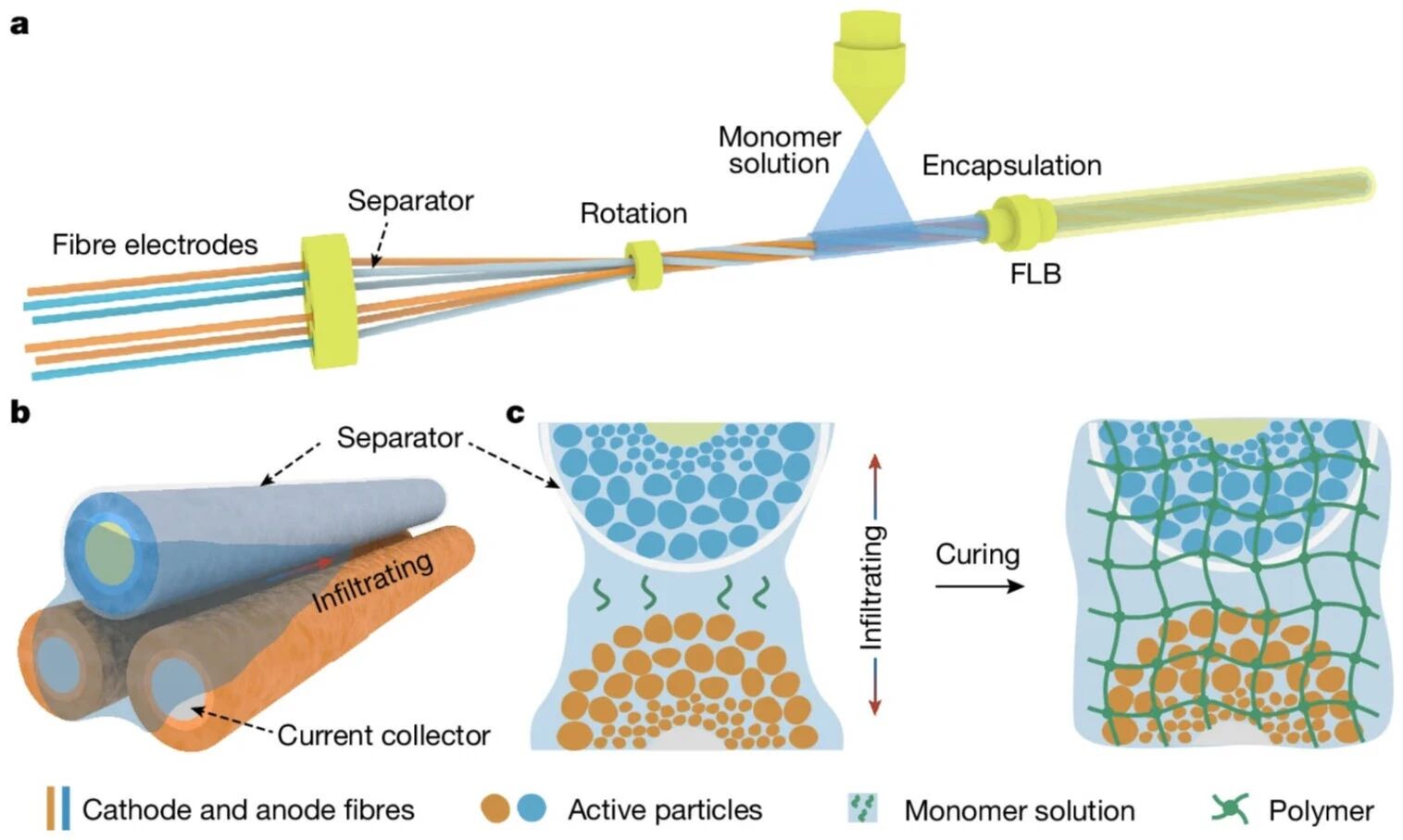
Qosim等(2025)解决的核心问题是:如何用一种更易实施、无需高电压的纤维制造路线,把传统上难以通过压力纺丝加工的CA做成药物释放的疏水核层,并与PVP壳层结合实现可编程双相释放。作者在引言中将这一技术路线定位为“简单且具产业化潜力”的工艺组合(Qosim等, 2025)。
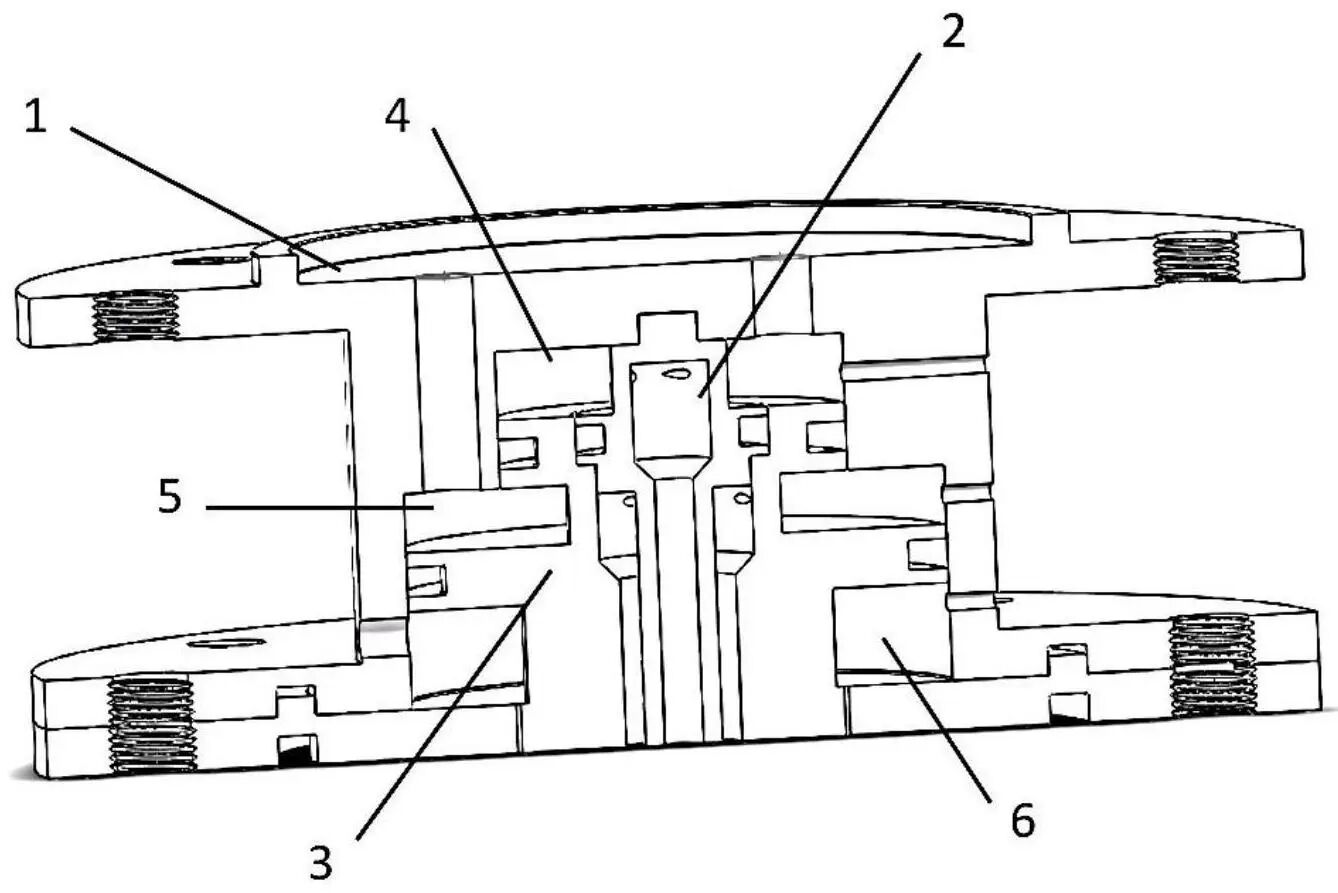
在实验设计上,作者使用铝制双腔旋转容器与同轴喷嘴(核/壳内径约0.65/2.2 mm),在0.1–0.3 MPa气压与12,000–32,000 rpm转速下纺丝30 s制得纤维;PVP用乙醇溶剂体系配制,CA用丙酮/水(约5:1)混合溶剂配制,并以2.5%、5%、7.5%(w/v)IBP作为载药梯度。随后用共聚焦荧光示踪验证核–壳结构,并通过“水中溶解除PVP壳层”估算核径与壳厚。
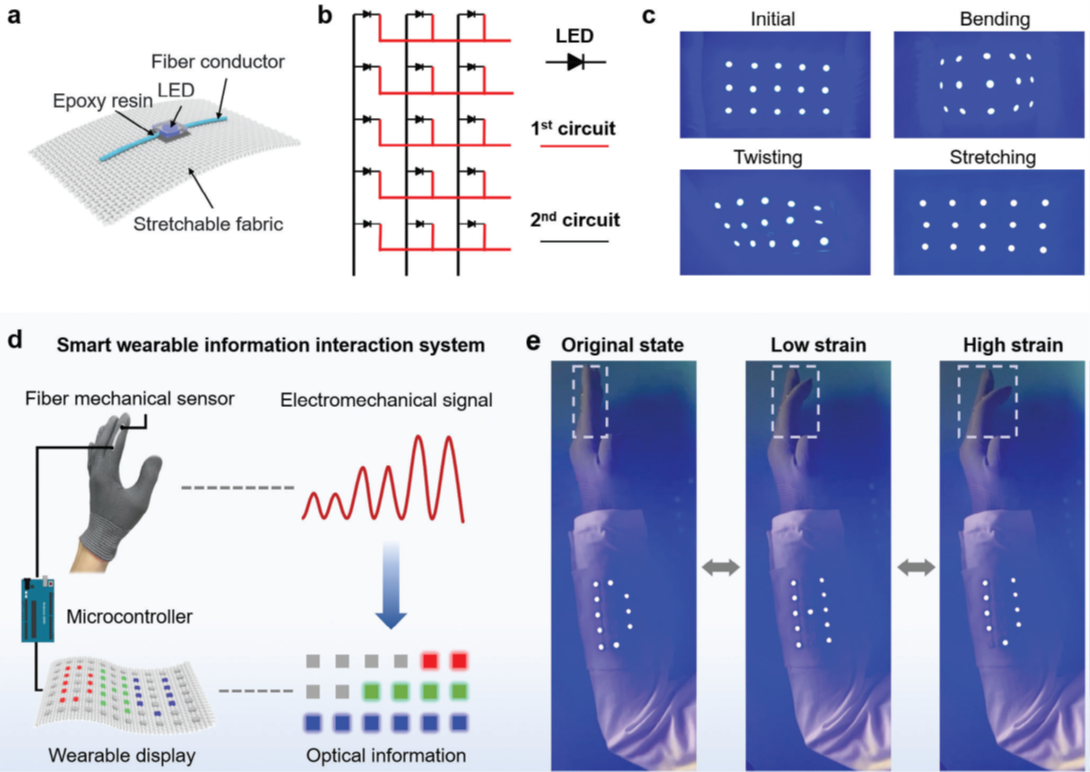
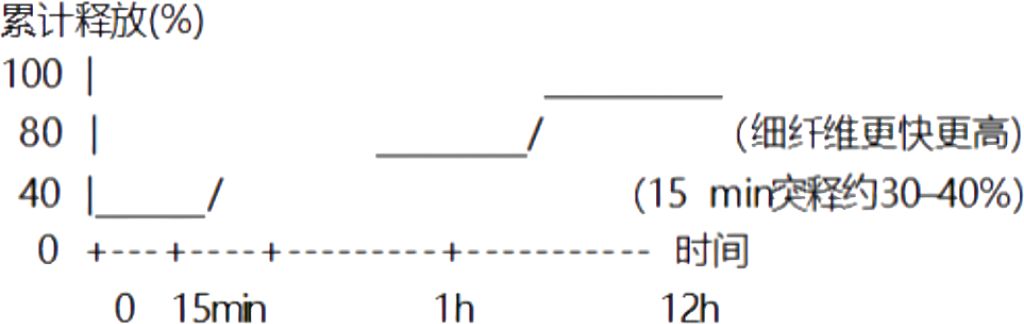
提高药物浓度会提高溶液黏度并显著增大纤维直径;而提高气压或转速可减小直径(最小约370nm,最大约1040 nm),核径与壳厚可达数百纳米量级。释药机制上,PVP壳层的高亲水性决定初期快速溶出(15 min约29–42%),随后由疏水CA核层主导扩散与维持释放;更细纤维因扩散路径更短而在12 h释放更多药物(例如约93% vs. 约62%)。固态表征(XRD/DSC/FTIR)支持药物在纤维中形成无定形固体分散并存在氢键相互作用;在温和室内条件贮藏8周后仍保持无定形与释放稳定。
该文的全文可通过ScienceDirect的DOI页面检索,同时UCL Discovery提供了开放获取版本的信息页。
PART 02
PVP的化学结构与理化性质
PVP(povidone/聚维酮)由1-乙烯基-2-吡咯烷酮(N-vinyl-2-pyrrolidone)自由基聚合形成线性聚合物,重复单元含内酰胺环与酰胺羰基,因而具有较强极性与氢键受体能力。药典条目通常用K值表征分子量/黏度等级(如K25、K30、K90);其典型性状为白色至微黄粉末、具引湿性,易溶于水与醇类溶剂,在丙酮中仅微溶、在乙醚中几乎不溶。
药剂功能
中国药典药用辅料条目明确将“聚维酮K30”归类为“黏合剂和助溶剂等”,并给出K值范围(约27.0–32.0)、残留单体(N-乙烯基吡咯烷酮)限度以及含水量、含氮量等质量指标;同时强调其需“遮光、密封、干燥处保存”。这些质量与贮存要求本质上都指向一个事实:PVP的吸湿与溶液黏度特性会直接影响其加工稳定性与产品一致性。
历史回顾

在PVP辅料专著的历史回顾中,PVP曾在二战时期被用作血浆代用品,但因机体不代谢该聚合物、肠外给药时少量高分子组分可能残留体内而在该用途上已停用;这一段历史提醒我们:当PVP从“口服/局部辅料”走向“高负载或新给药途径”的先进递送材料时,分子量分布、残留单体与杂质谱将是不可回避的风险评估点。
主要优势
PVP在药物递送中的“结构—性质”优势主要体现在:亲水溶解与界面润湿可加快难溶药物溶出;快速溶剂挥发工艺(电纺/压力纺丝等)可把药物锁定为无定形固体分散;而其强吸湿性又可能塑化无定形体系、降低玻璃化温度并增加分子运动性,从而提高相分离或重结晶风险。
下表从“药物递送载体”的工程指标出发,对比PVP与PCL、PLA、PEG等常见高分子在关键属性上的差异,用于解释为什么“疏水核层+亲水PVP壳层”天然适合构建快–慢双相曲线
【表中归纳基于药典与综述文献的“典型趋势”,具体表现仍受分子量、共聚/交联方式与剂型工艺影响。】
PART 03
核–壳纳米纤维中的PVP功能与制备机理
PART 04
药物递送与生物医用材料应用图景
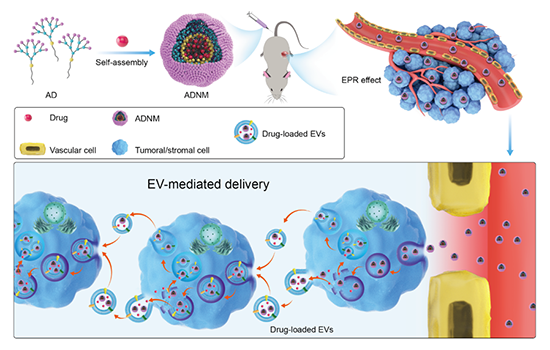
对PVP而言,“可降解长效骨架”并非其最突出的优势;它更常作为亲水载体、增溶与快速溶出相来使用。典型用法包括:将难溶药物制成无定形固体分散体以提高溶出;在局部给药贴片与快速溶出纤维中实现快速起效;以及在核–壳结构中作为可溶壳层实现分段释放(Zupančić等, 2019;Qosim等,2025)。
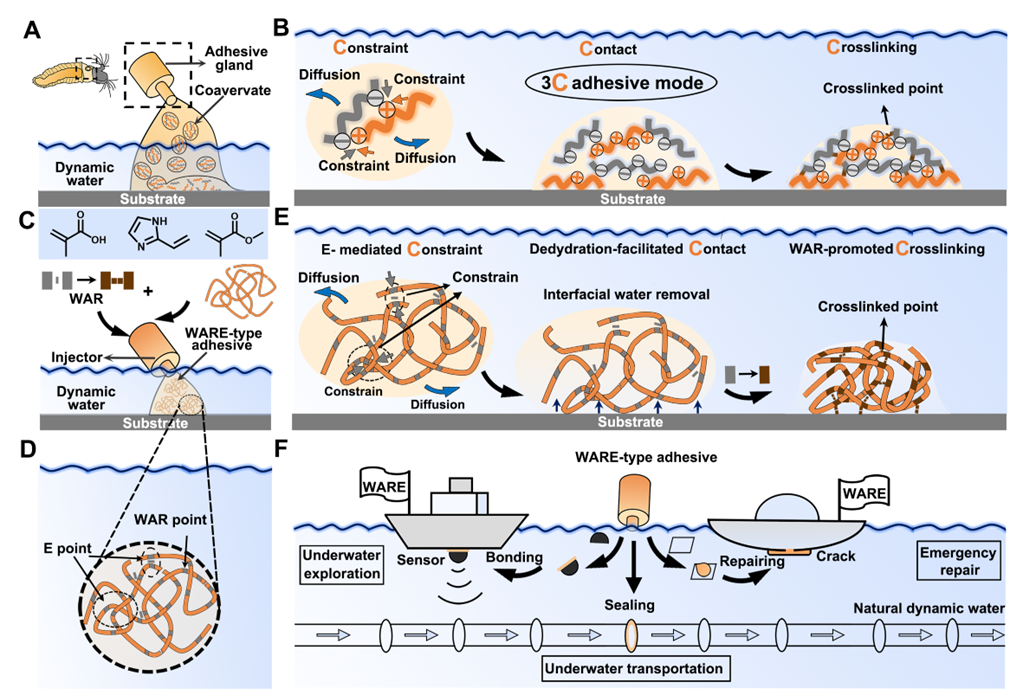
在传统固体制剂领域,中国药典药用辅料条目对聚维酮K30的K值、残留单体、含水量与贮藏条件提出明确要求;交联聚维酮(crospovidone)则通过毛细吸水(wicking)机制等作为“超级崩解剂”促进片剂崩解与溶出。若从“水传输与界面润湿”这一统一机理出发,纤维体系中PVP壳层的快释与片剂体系中PVP/交联PVP的促崩解,其实共享同一类材料优势:高极性内酰胺结构+高比表面积形态放大水分进入与药物溶出过程。
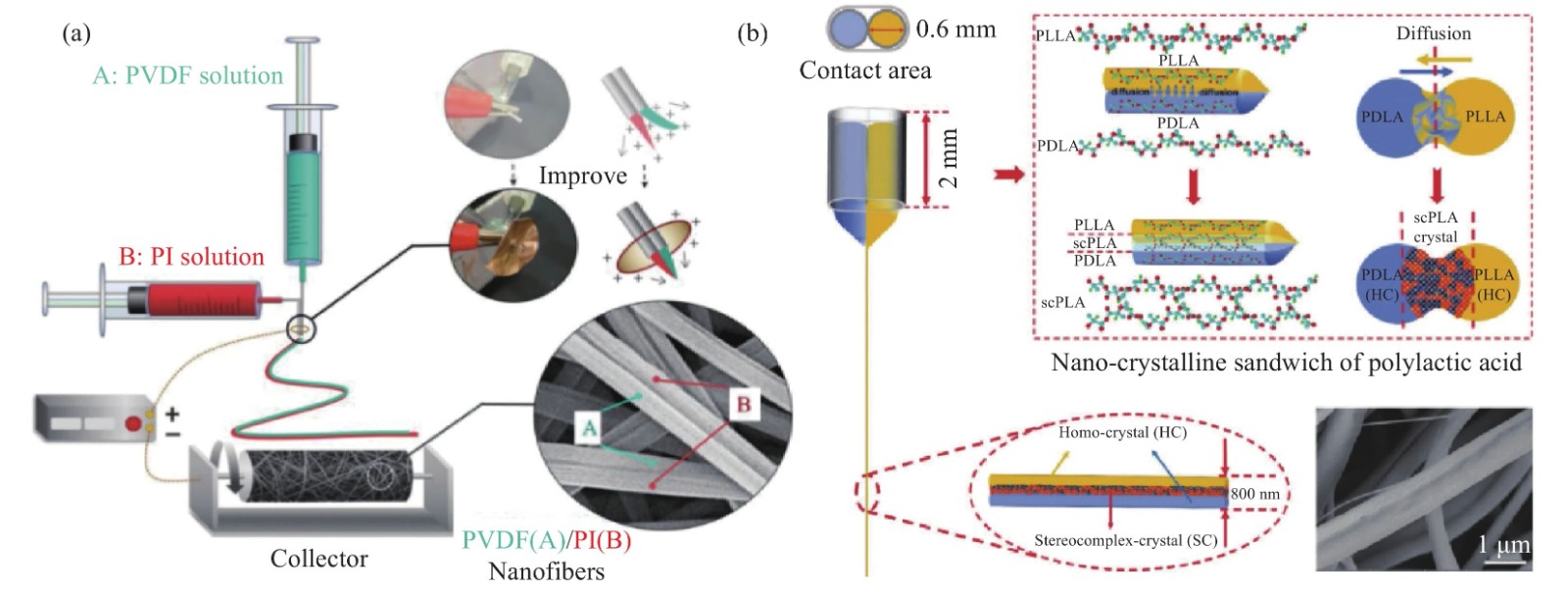
对产业化而言,压强旋纺/压力纺丝类方法因无需高电压装置而被认为更易放大;但文献也指出其纤维细度与均一性控制往往不如电纺,存在“产率/易放大”与“精细可控”之间的权衡。因此,若要把PVP核–壳纤维从实验室推进到产品化,结构一致性与批间释放一致性应被视为首要工程目标。
PART 05
优势、局限与关键挑战
PVP体系的优势与局限常来自同一根源:亲水性与吸湿性。
研究表明高吸湿聚合物可能增加体系含水量并影响无定形相的相行为;在高湿暴露条件下,含PVP的无定形固体分散体可出现非均相化并继发结晶的过程,提示“湿度—分子运动性—结晶—释药漂移”是一条必须被量化管理的风险链。作为对照,Qosim等在相对温和的室内储存条件下观察到8周稳定性,但原文未覆盖更苛刻湿热条件或更长货架期,因此仍需在加速稳定性框架下验证可迁移性。
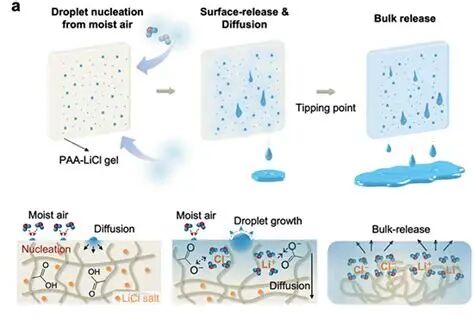
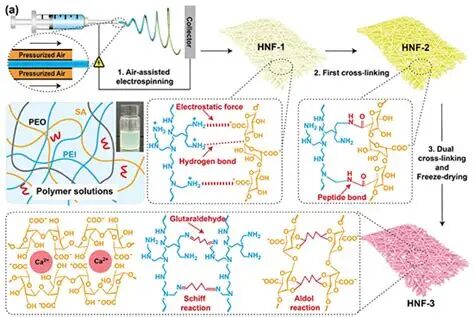
PVP辅料专著指出机体通常不代谢PVP,肠外给药时高分子量组分可能残留体内的历史关切提示应结合给药途径与分子量等级进行风险评估。另一方面,虽然罕见,仍有与聚维酮相关的过敏/过敏性休克病例报告,提示在特定人群与暴露方式下应把“辅料致敏”纳入风险管理。
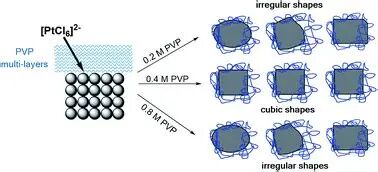
核–壳纤维的关键质量属性(CQA)应至少覆盖:直径分布、核径/壳厚统计、药物固态(无定形程度)、残留溶剂与释放曲线批间一致性。Qosim等通过共聚焦示踪与选择性溶解除壳估算壳厚,为建立“结构一致性→释放一致性”的质量框架提供了可操作的实验路径。
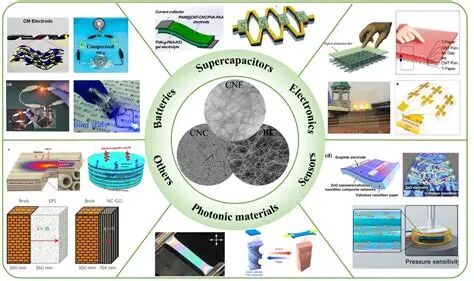
药典为PVP(povidone/聚维酮)提供了基础质量约束:例如《The JapanesePharmacopoeia 》(JP XIV)给出其溶解性、吸湿性等描述,而中国药典条目给出K值范围与残留单体限度,并可见国家药典委员会曾就聚维酮K30辅料标准修订公开征求意见。与此同时,U.S. Food and Drug Administration 提供“非活性成分数据库(IIG)”下载与查询入口,可用于按给药途径追溯辅料既往使用先例。
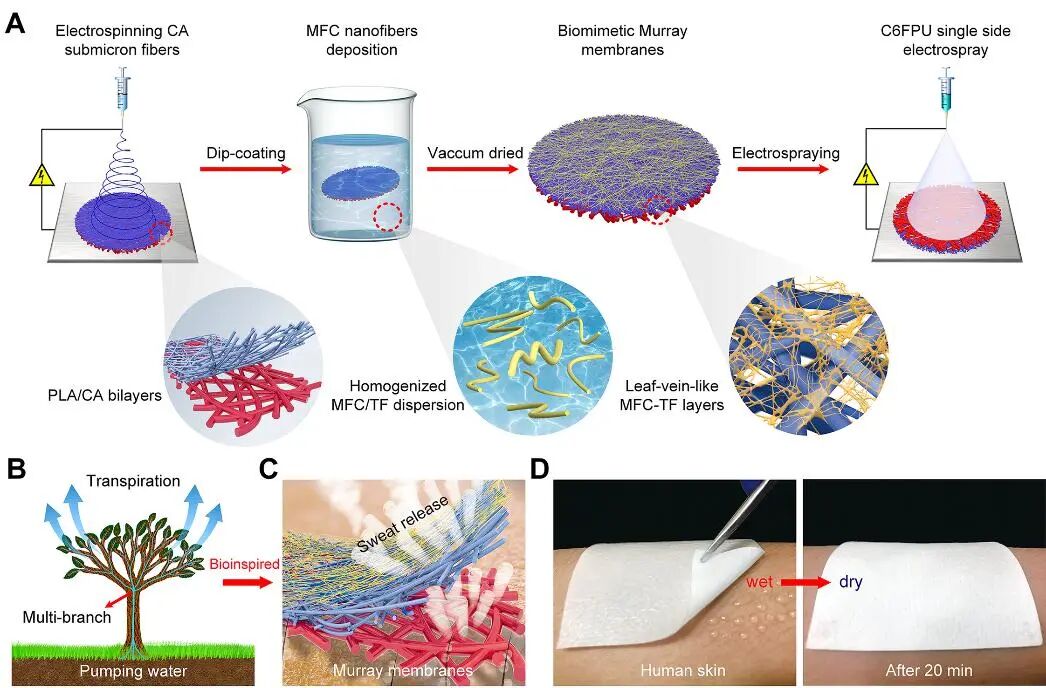
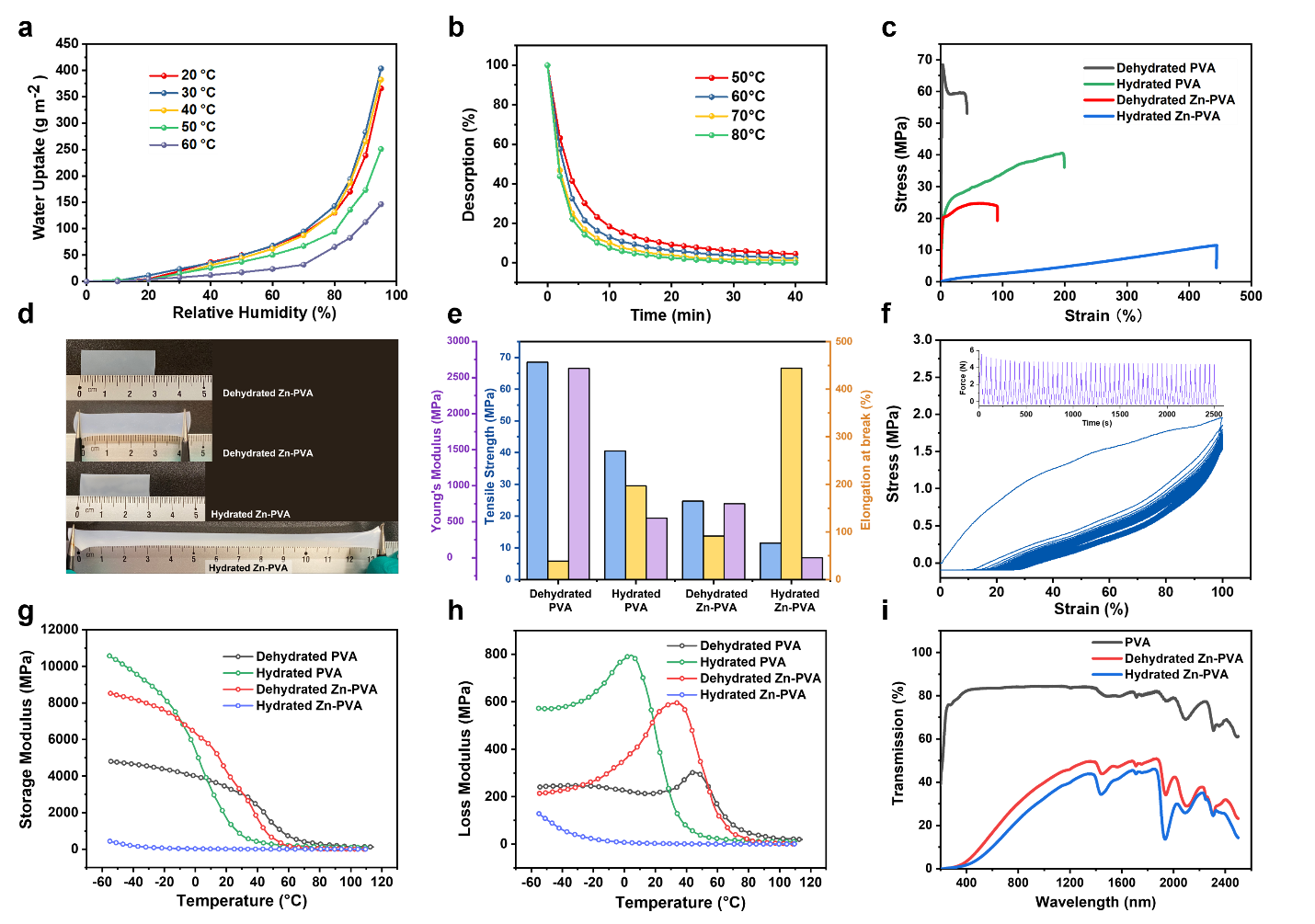
PART 06
未来方向、产业化前景与结论建议
以Qosim等(2025)的证据链为起点,PVP核–壳纤维平台的下一步应从“概念验证”转向“可预测与可放大”。特别是:把吸湿性带来的不确定性转化为可工程化的稳定性设计;把工艺参数与微结构的耦合关系统一到质量体系;并尽早用体内相关性验证“双相释放”的临床价值。
研究建议
面向湿度敏感性开展“屏障工程”:
在不牺牲PVP快释优势的前提下,引入超薄疏水涂层/外层屏障或包装策略,量化湿度对无定形稳定性与释放曲线漂移的影响。
建立“结构–性能”模型:
以壳厚、核径、直径分布(CV)与无定形程度为输入变量,拟合突释比例与维持段速率,形成工艺设计图谱并用于放大时的批间一致性控制。
尽早验证体内相关性:
围绕起效时间与维持浓度等终点建立IVIVC或体外–体内趋势一致性评价,同时将PVP分子量等级、残留单体与潜在致敏风险纳入给药途径选择与说明书风险管理。
总结
总体而言,PVP凭借亲水溶解、成纤加工友好与无定形固体分散能力,在核–壳纳米纤维中可被精准用作“快释功能层”;当其与疏水核层、可放大的压力纺丝工艺以及结构一致性的质量体系结合时,有望形成兼具性能可编程与制造可放大的药物递送材料平台。

聚乙烯吡咯烷酮
PVP
PVP业之先锋
021-50565706